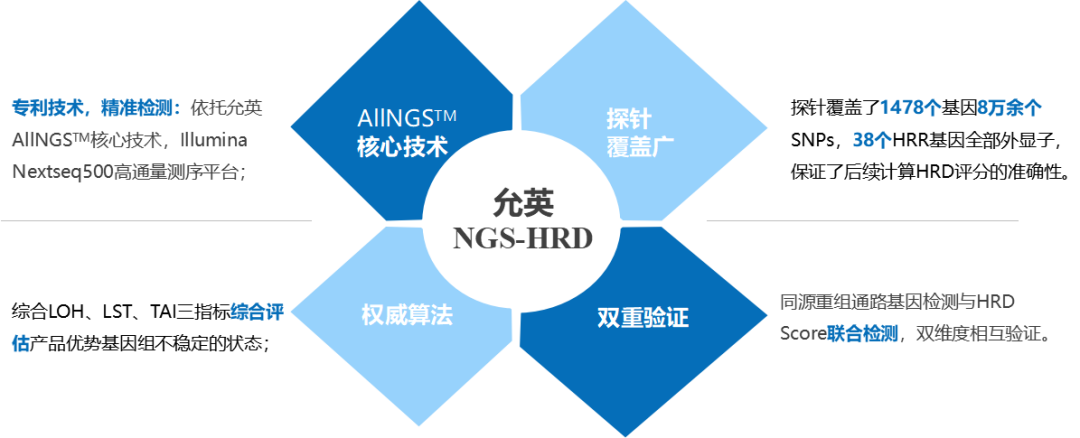
通过检测杂合性缺失(LOH)、端粒等位基因失衡(TAI)及大片段移位(LST)综合得分来评估HRD状态,同时还提供包括BRCA1/2等HRR相关基因的检测结果,全面评估卵巢癌等患者对PARP抑制剂的敏感性。
发生HRD的肿瘤细胞不能准确地修复DNA,转而依赖其他易错的途径来修复DNA, 这一缺陷导致基因组疤痕。
常见的基因组疤痕有三种类型:基因组杂合性丢失(LOH, loss of heterozygosity)、端粒等位基因失衡(TAI,telomeric allelic imbalance)和大片段迁移(LST,large-scale state transitions)。通过计算LOH+TAI+LST的分值,进而评估HRD状态。
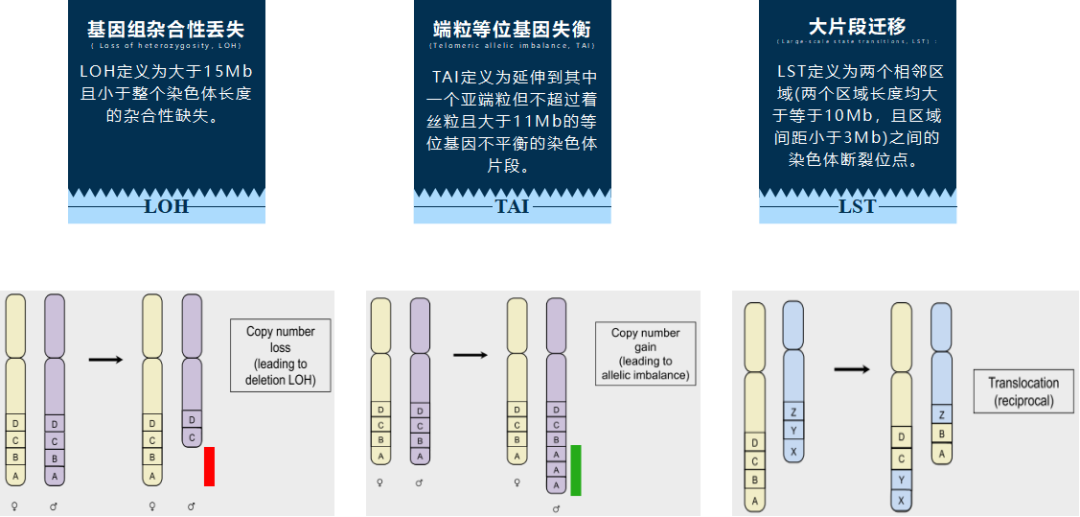
HRR通路基因突变等因素可导致HRD的发生。
发生HRD的肿瘤细胞由于不能准确的修复DNA损伤依赖其他易错的途径来修复DNA, 这一缺陷导致基因组疤痕。
即HRR相关基因突变检测是从导致HRD的“因”来检测HRD,基因组疤痕分析则是从HRD引起的“果”来检测HRD。
为什么要检测HRD?
PROfound等多项研究数据显示HRR基因改变可以提示卵巢癌、乳腺癌、前列腺癌、胰腺癌等患者对PARP抑制剂药物治疗的敏感性。
1. 卵巢癌
HRD检测可以使卵巢癌患者PARP抑制剂敏感人群从占20%左右的BRCA突变人群扩大到占50%左右的HRD阳性人群。
PAOLA-1研究显示,在HRD阳性组(包括BRCA突变的患者)的卵巢癌患者中,奥拉帕利联合贝伐珠单抗一线维持治疗组的mPFS为37.2个月,贝伐珠单抗单药治疗组mPFS为17.7个月,同时联合治疗组疾病进展和死亡的风险降低67%。
国内外多个指南建议卵巢癌患者检测HRD,指导奥拉帕利等PARP抑制剂治疗。

2、乳腺癌
HRD阳性乳腺癌多见于三阴性乳腺癌,BRCA1/2 基因胚系突变是导致乳腺癌 HRD最常见的原因,PALB2的生殖系突变以及BRCA1和RAD51的启动子甲基化等也会引起HRD。
TBCRC 048研究显示PALB2胚系突变(gPALB2,ORR=82%)和sBRCA(ORR=50%)突变的患者中观察到PARP抑制剂明确的应答。
3、前列腺癌
美国FDA已批准奥拉帕利用于治疗经新型内分泌治疗后进展且携带HRR突变的mCRPC患者(ATM、BRCA1、BRCA2、BARD1、BRIP1、CDK12、CHEK1、CHEK2、FANCL、PALB2、RAD51B、RAD51C、RAD51D、RAD54L);批准卢卡帕利治疗经新型内分泌治疗和多西他赛化疗后进展且携带BRCA突变的mCRPC患者。
PROfonnd研究显示奥拉帕利显著改善携带HRR基因突变转移性前列腺癌患者无进展生存期和总生存期。
4、胰腺癌
美国FDA批准PARP抑制剂奥拉帕利(olaparib)作为接受含铂一线化疗方案至少16周病情仍未进展、携带有害或疑似有害胚系BRCA突变(gBRCAm)的转移性胰腺癌成人患者的一线维持治疗。既往研究发现,约4-7%的胰腺癌患者携带胚系BRCA1/2突变,这些患者对铂类药物尤其敏感。
POLO研究结果显示奥拉帕利组相比安慰剂组,中位PFS显著延长(7.4个月 vs 3.8个月,HR=0.53,P=0.0038),疾病进展风险降低47%。
允英HRD检测项目
允英NGS-HRD 通过同源重组通路基因检测与HRD Score联合检测,双维度相互验证。
通过检测杂合性缺失(LOH)、端粒等位基因失衡(TAI)及大片段移位(LST)综合得分来评估HRD状态,同时还提供包括BRCA1/2等HRR相关基因的检测结果,全面评估卵巢癌等患者对PARP抑制剂的敏感性。HRD状态判定:
允英NGS-HRD项目采用国际HRD评判标准,结合通过生物信息学权威算法,从LOH、TAI和LST三个方面分析样本DNA同源重组修复缺陷(HRD)情况,统计HRD评分,同时结合BRCA1/2基因的突变情况,最终如果HRD评分大于等于42或者检出BRCA1/2突变,即认定该患者为HRD阳性,反之则为阴性。
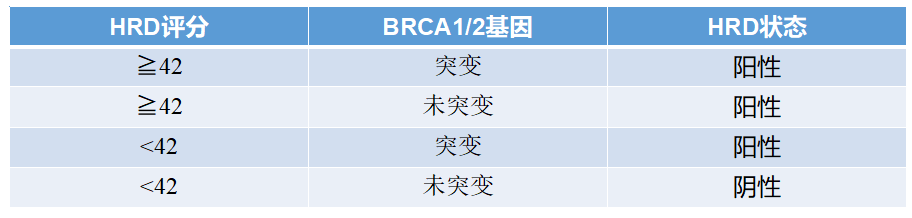
允英NGS-HRD 样本类型
肿瘤组织(新鲜手术组织/穿刺组织/FFPE肿瘤组织石蜡切片[保存时间一年以内])
Ø 精准指导卵巢癌/乳腺癌/前列腺癌/胰腺癌/PARP抑制剂及铂类用药
肿瘤组织(新鲜手术组织/穿刺组织/FFPE肿瘤组织石蜡切片[保存时间一年以内])+ 全血(对照血)适用人群
·卵巢癌、胰腺癌、前列腺癌、乳腺癌患者;·既往检测BRCA1/2检测阴性,寻求PARP抑制剂获益的患者。
检测优势